Книга 1. От огня и воды к электричеству
Раздел 8. Нефть и газ
Нафти – це природні маслянисті горючі рідини зі своєрідним запахом. Вони мають різноманітну консистенцію – від легкоплинних до густих, малорухомих. Колір нафт у більшості випадків бурий і темнокоричневий (до чорного), рідше жовтий і зеленуватий і зовсім рідко зустрічається майже безбарвна, так звана «біла нафта». Колір нафт залежить від розчинених в них смол. Нафта являє собою суміш рідких вуглеводнів (парафінових, нафтенових і ароматичних), в якій розчинені газоподібні та тверді вуглеводні. У незначних кількостях вона містить сірчані й азотні сполуки, органічні кислоти та деякі інші хімічні сполуки.
З фізичної точки зору нафта розглядається як розчин газоподібних і твердих вуглеводнів у рідині. Природна нафта, що добувається з надр Землі, завжди містить певну кількість розчинених у ній газів (супутні природні гази), головним чином метану і його гомологів.
Аналіз нафт з виділенням індивідуальних сполук вимагає багато часу. У технологічних розрахунках при визначенні якості сировини, продуктів нафтопереробки і нафтохімії часто використовуються дані технічного аналізу, який полягає у визначенні деяких фізичних, хімічних й експлуатаційних властивостей нафтопродуктів. З цією метою використовують наступні методи, що в комплексі дають можливість охарактеризувати товарні властивості нафтопродуктів у різноманітних умовах експлуатації, пов'язати їх зі складом продуктів, що аналізуються, дати рекомендації щодо найбільш раціонального їх використання:
• фізичні – визначення густини, в'язкості, температури плавлення, замерзання і кипіння, теплоти згоряння, молекулярної маси, а також деяких умовних показників (пенетрація, дуктильність);
• хімічні, що застосовують класичні прийоми аналітичної хімії;
• фізико-хімічні – колориметрія, потенціо-метричне титрування, нефелометрія, рефрактометрія, спектроскопія, хроматографія;
• спеціальні – визначення октанового і метанового чисел моторного палива, хімічної стабільності палив і масел, корозійної активності, температури спалаху і займання та ін.
Густина. Нафти розрізняються за густиною, тобто за масою, що міститься в одиниці їх об'єму. Якщо в посудину з нафтою налити воду, то, за винятком рідкісних випадків, нафта спливає. Зазвичай вона легша за воду. Густина нафти, виміряна при температурі 20°С, віднесена до густини води, виміряної при 4°С, називається відносною густиною нафти. Визначення густини можна проводити при будь-якій температурі, а потім вирахувати значення відносної густини, використовуючи коефіцієнт об'ємного розширення, значення якого наводяться у довідковій літературі.
Відносна густина нафт коливається в межах 0,5–1,05 кг/дм3 (зазвичай 0,82–0,95). Нафти з відносною густиною до 0,85 називаються легкими. Своєю легкістю вони зобов'язані переважанню в їх складі метанових вуглеводнів. Відносну густину від 0,85 до 0,90 мають середні нафти, а вище 0,90 – важкі. У важких нафтах містяться переважно циклічні вуглеводні.
Густина нафти залежить від багатьох факторів: хімічної природи речовин, що до неї входять, фракційного складу, кількості смолистих речовин, кількості розчинених газів та ін. Густина нафти залежить від глибини залягання, як правило, зменшуючись з її збільшенням. Винятки з цього правила пояснюють вторинними явищами, наприклад міграцією легких нафт у більш високі горизонти залягання.
При визначенні густини нафт і нафтопродуктів звичайно користуються кількома методами: за допомогою ареометрів (нафтоденсиметрів), методом зваженої краплі, за допомогою гідростатичних ваг, пікнометричним методом (найбільш точний).
У поєднанні з іншими показниками (коефіцієнт заломлювання, молекулярна маса) густина використовується для визначення вуглеводневого чи структурно-групового складу нафтових фракцій.
В'язкісні властивості. При видобутку і транспортуванні нафти велике значення має така її властивість, як в'язкість. Розрізняють динамічну і кінематичну в'язкість. Динамічною в'язкістю називається внутрішній опір (тертя) окремих часток рідини руху загального потоку.
У легких нафт в'язкість менша, ніж у важких. Вона зменшується також з підвищенням температури, оскільки при цьому збільшується відстань між молекулами. Тому при видобуванні та подальшому транспортуванні трубопроводами важкі нафти вимагають підігріву. При 80–100°С в'язкість важких нафт наближається до в'язкості легких.
Для характеристики в'язкості нафт і нафтопродуктів на практиці найбільш широко використовується кінематична в'язкість, що дорівнює відношенню динамічної в'язкості до густини рідини при температурі визначення.
В'язкість дуже суттєво залежить від температури, тому завжди вказується температура її визначення. В'язкість нафти при 50°С коливається в межах 1,2–55 сСт (сантистоксів) і залежить від її хімічного і фракційного складу, вмісту асфальто-смолистих речовин. Чим легший фракційний склад нафти і чим вища її температура, тим нижча в'язкість; чим більше асфальто-смолистих речовин, тим вона вища.
Поверхневий натяг. Поверхневим натягом (густиною поверхневої енергії) називається відношення роботи, необхідної для збільшення площі поверхні, до величини цього приросту густини. Для різних нафт поверхневий натяг на межі з повітрям коливається в межах 25–30 мН/м.
Нафтопродукти, слабко очищені від полярних домішок, мають низький поверхневий натяг на межі з водою. Для добре очищених бензинів і масел (медичне, трансформаторне) значення поверхневого натягу складають до 50 мН/м. Що стосується залежності поверхневого натягу нафтопродуктів від їх хімічного складу, то при однаковому числі вуглеводних атомів у молекулі (С6) найбільшим поверхневим натягом при температурі 20°С володіють ароматичні вуглеводні, найменшим – метанові, а нафтенові й олефінові вуглеводні займають проміжну позицію.
Поверхневий натяг вуглеводнів і нафтових фракцій є лінійною функцією температури. З підвищенням температури він зменшується і при критичній температурі дорівнює нулю. Із збільшенням тиску поверхневий натяг у системі газ–рідина зменшується.
Тверднення і плавлення, загусання і розм'якшення, випаровування, кипіння і перегонка. У нафт і нафтопродуктів, як у складних сумішей, немає якоїсь однієї точки тверднення чи точки плавлення. Для них характерна наявність лише температурних інтервалів як тверднення, так і плавлення. Тверднення і плавлення нафтопродуктів завжди супроводжуються проміжними стадіями – загусанням і розм'якшенням.
Рідка нафта звичайно затвердіває біля –20°С, але іноді вона загусає навіть при незначному охолодженні (температура приблизно +11°С). Чим більший вміст у нафті твердих парафінів, тим при порівняно більш високій температурі вона застигає.
Найменшу температуру твердення (до –80°С і нижче) мають бензини, потім – у порядку зростання цієї температури – розміщуються керосини, легкі й важкі масла.
З явищем випаровування нафт і нафтопродуктів доводиться рахуватися здебільшого при їх зберіганні та транспортуванні.
Оскільки нафта і нафтопродукти являють собою вельми складні суміші різних вуглеводнів і невуглеводневих сполук з різними температурами кипіння, то мова може йти лише про температурні межі, в яких википає та чи інша суміш. Температура кипіння нафти коливається в інтервалі 50–550°С.
Природні речовини можуть знаходитися в трьох агрегатних станах: твердому, рідкому і газоподібному, а також мати вигляд плазми. Кожний агрегатний стан характеризується певною внутрішньою структурою речовини і відповідно певними властивостями. При переході з твердого стану в рідкий відбувається плавлення, при переході з рідкого в газоподібний –випаровування. У твердому тілі молекули речовини коливаються щодо своїх положень рівноваги в кристалічній решітці. Якщо кристалу надати енергію, коливання посилюються і кристалічна решітка може зруйнуватися. Фазовий перехід з твердого стану в рідкий відбувається при певній, залежній від тиску температурі. Зазвичай температура плавлення підвищується із зростанням тиску.
У рідинах молекули пов'язані між собою молекулярними силами зчеплення. При підводі енергії до рідини тепловий рух молекул посилюється і ці сили вже не можуть утримати молекули в рідині. Фазовий перехід з рідкого в газоподібний стан відбувається при певній (сильно залежній від тиску) температурі, яку називають температурою кипіння.
Нафта, як і будь-яка рідина, при певній температурі закипає і переходить в газоподібний стан. Різні її компоненти переходять у газоподібний стан при різній температурі кипіння.
Легкі нафти закипають при 50–100°С, важкі – при температурі більше 100°С. Найвища температура кипіння у парафінів, тому при зниженні температури вони випадають з нафти в осад. При видобуванні нафти з високотемпературних пластових умов на поверхню землі стовбуром бурової свердловини парафіни відкладаються на стінах труб.
Різниця температур кипіння вуглеводнів, що входять до складу нафт, широко застосовується на практиці для поділу нафти на температурні фракції (франц. «фрактьон» – частка, частина від лат. «фракціо» – злом, ломка). Так, при нагріванні нафти до 180–200 °С википають вуглеводні бензинової фракції, при 200–250 °С – лігроїнової, при 250–315 °С – керосиново-газойлевої і при 315–550 °С – масляної. Залишок представлений гудроном. До складу бензинової та лігроїнової фракцій входять вуглеводні, що містять 6–10 атомів вуглецю. Керосинова фракція складається з вуглеводнів з С11 – C13, газойлева – з Cl4 – C17 і так далі.
Звичайно нафти густиною менше 0,9 починають кипіти при температурі, нижчій 100°С. Температура початку кипіння нафти залежить від її хімічного складу. Так, при одній і тій же густині нафтенові та ароматичні вуглеводні киплять при більш низькій температурі, ніж метанові.
Розчинність і розчинювальна здатність. З водою ні нафти, ні нафтові вуглеводні практично не змішуються, а їх обопільна розчинність дуже мала і не перевищує сотих часток відсотка. Однак варто розрізняти розчинність нафтопродуктів і вуглеводнів у воді та, навпаки, розчинність води в нафтопродуктах і нафтових вуглеводнях. Розчинність нафтопродуктів у воді вкрай низька і зменшується від бензинів до більш важких продуктів – керосинів і мастил. З підвищенням температури (до критичної) вона збільшується.
У нафтових вуглеводнях вода розчиняється у незначній кількості – від 0,003 до 0,13% (мас.) при 40°С. У найбільшій кількості вода розчиняється в неграничних вуглеводнях. Близькі до останніх за розчинювальною здатністю й ароматичні вуглеводні. Найменшу кількість води розчиняють метанові вуглеводні. Із збільшенням молекулярної маси розчинювальна здатність всіх вуглеводнів стосовно води зменшується.
Розчинність води в бензинах помітно більша, ніж розчинність бензинів у воді. Із збільшенням густини нафтопродуктів розчинність води в них різко знижується. Для одного і того ж нафтопродукту розчинність води зростає з підвищенням температури.
Обопільна розчинність води і нафтопродуктів має велике практичне значення, наприклад, у зв'язку з можливістю виділення з моторного палива у вигляді мікрокрапель розчиненої в ньому води чи кришталиків льоду, що здатні ускладнювати роботу двигунів.
Важливою є властивість нафт розчиняти вуглеводневі гази. У 1 м3 нафти може розчинитися до 400 м3 горючих газів, що приблизно в 10 разів більше розчинності природного газу у воді.
За співвідношенням вмісту метану і його гомологів природні вуглеводневі гази поділяються на сухі та жирні. У сухому газі переважає метан – 98,8%, у жирному – до 50% складають етан, пропан, бутан і вищі вуглеводні. Жирний газ розчиняється в нафті краще, ніж сухий.
За певних умов рідкі вуглеводні можуть розчинятися в газі. Якщо об'єм газової фази значно перевищує об'єм нафти, то при підвищенні тиску до 20–25 МПа і температурі 90–95°С рідкі вуглеводні можуть перейти в пароподібний стан (випаровуватися) і розчинитися в газі. Ця властивість рідких вуглеводнів, на протилежність процесу розчинення (конденсації) вуглеводневих газів у нафті, називається зворотним, або ретроградним (лат. «ретро» – назад, у зворотний бік) випаровуванням. Такі умови мають місце на глибині, в надрах Землі. При видобуванні газу на поверхню температура і тиск різко знижуються і з газової суміші починає випадати конденсат у вигляді рідких вуглеводнів. Це явище називається зворотною конденсацією. Газові поклади, в яких нафта знаходиться в пароподібному стані й насичує вільний газ, називаються газоконденсатними. Вміст конденсату в таких покладах коливається від 50 до 300–400 см3/м3.
Молекулярна маса. Молекулярна маса – найважливіша характеристика нафти і нафтопродуктів. Цей показник дає «середнє» значення молекулярної маси речовин, що входять до складу тієї чи іншої фракції нафти, і дозволяє зробити висновок про склад нафтопродуктів. Він широко застосовується для розрахунків апаратури нафтопереробних заводів. Молекулярна маса пов'язана з температурою кипіння продуктів і використовується для визначення молекулярної рефракції, парахору (емпірична залежність, що дозволяє охарактеризувати хімічний склад нафтових фракцій) та ін.
Молекулярну масу нафтопродуктів, як і індивідуальних речовин, визначають різними методами, що пояснюється різноманітністю властивостей цих продуктів. Молекулярна маса визначається кріоскопічним методом – за зниженням температури кристалізації розчину досліджуваного продукту, наприклад у бензолі, нітробензолі та ін.; ебуліоскопічним – за підвищенням точки кипіння (у випадку легких нафтових фракцій); методом Раста – за зниженням температури плавлення сплаву досліджуваної речовини з камфорою, бензойною кислотою, дифеніламіном та ін. (для більш висококиплячих нафтопродуктів). Крім того, молекулярну масу нафтопродуктів можна розраховувати за емпіричними формулами. Найчастіше використовується формула Б.П. Войнова:
М = а + bt + сt2,
де t – середня температура кипіння продукту, °С; а, b, с – постійні, числові значення яких різні для кожної групи вуглеводнів.
Теплові властивості. Найголовнішою властивістю нафти і горючих газів, яка принесла їм світову славу виняткових енергоносіїв, є їх здатність виділяти при згорянні значну кількість теплоти. Теплотою згоряння називається відношення кількості теплоти, що виділяється при горінні, до маси вигорілого до кінця (тобто до утворення вуглекислоти СО2 і води Н2О) палива.
Нафта, природний горючий газ та їх похідні мають найвищу серед всіх типів палива теплоту згоряння. Теплота згоряння нафти – 41 МДж/кг – в 1,3 більша теплоти згоряння кращих сортів кам'яного вугілля – 31 МДж/кг; теплота згоряння бензину – 42 МДж/кг; дизельного палива – 42,7 МДж/кг, етану, пропану і бутану – відповідно 64,5;
93,4 і 124, а природного газу – 35,6 МДж/м3.
Теплоту згоряння нафти, керосину та інших нафтопродуктів визначають у калориметричній бомбі, а газів – в газовому калориметрі. Для нафт теплота згоряння коливається у вузьких межах: від 40000 до 45000 кДж/кг, причому отримувана величина тим більша, чим менша густина нафт (і відповідно їх фракцій). Теплота згоряння нафтопродуктів залежить також від особливостей їх вуглеводневого складу. Приблизно з похибкою 3–5% теплоту згоряння нафт і нафтопродуктів можна вирахувати за допомогою різноманітних емпіричних формул, наприклад за даними їх елементного аналізу (Д.І. Менделєєв), а також за їх густиною (формула Крего).
Колір, флуоресценція і люмінесценція. Колір нафт залежно від їх хімічного складу може бути різним. Чим більше в нафті смол і особливо асфальтенів, тим забарвлення її за глибиною чи відтінком більш темне. Легкі нафти густиною 0,78–0,79 кг/дм3 мають жовте забарвлення, нафти середньої густини (0,79–0,82 кг/дм3) – бурштинового кольору і важкі – темно-коричневі та чорні.
Більшість нафт, а також їх фракції володіють флуоресценцією: вони мають синюватий або зеленуватий колір у відбитому світлі. Ця властивість пов'язана з присутністю в нафтах багатоядерних вуглеводнів ароматичного ряду.
Велике значення як метод аналізу під час геологічних пошуків нафти має люмінесценція (лат. «люменесценцо» – той, що світиться), тобто свічення нафт і нафтових бітумів, що виникає при опроміненні їх ультрафіолетовими променями. Під час пошуків нафти навіть незначні її сліди у гірських породах можуть бути виявлені за допомогою люмінесцентного аналізу. При цьому легкі нафти світяться інтенсивно блакитним кольором, а важкі – бурим і жовто-бурим. Відомо, що вуглеводні, які складають нафтові фракції з температурою кипіння до 300°С, а також парафіни і асфальтени не випромінюють світла у видимій частині спектру під дією ультрафіолетових променів. На відміну від цього до люмогенних речовин належать нафтенові кислоти, поліциклічні ароматичні вуглеводні та смоли.
Оптичні властивості. Майже всі нафти мають властивість обертати площину поляризації променів світла, причому для більшості їх характерне слабке праве обертання. Ця властивість визначається за допомогою поляриметрів.
Оптична активність зростає з підвищенням температури кипіння фракції, тобто збільшенням молекулярної маси. Зовсім не обертають площину поляризації бензинові фракції нафти, малою оптичною активністю володіють нафти, багаті на метанові й нафтенові вуглеводні, а також смоли і нафтенові кислоти. Ця властивість здебільшого притаманна, очевидно, складним чи гібридним нафтеноароматичним вуглеводням. Штучні нафти на відміну від природних оптичної активності не виявляють.
Електричні властивості. Нафта і нафтопродукти не проводять електричний струм, вони є діелектриками і характеризуються надзвичайно високим електричним опором. Наприклад, для парафіну він складає від 2 до 0,3·108 Ом·м. Деякі з них застосовуються в електротехнічній промисловості та радіотехніці як ізоляційний матеріал (парафін) чи ізолююче середовище (трансформаторні масла) в трансформаторах, масляних реостатах і вимикачах.
І нафта, і нафтопродукти при терті (в процесі заповнення сховищ і перекачування з великою швидкістю по трубах, а також фільтрації) легко електризуються і на їх поверхні можуть утворюватися й накопичуватися заряди статичної електрики, у зв'язку з чим можуть відбуватися вибухи і пожежі. Найбільш небезпечні щодо цього світлі нафтопродукти, які добре накопичують статичну електрику. Для запобігання небезпеки вибухів апаратуру, резервуари і трубопроводи заземляють, а також застосовують спеціальні антистатичні присадки у нафтопродуктах.
Діелектрична проникність нафт і нафтопродуктів у порівнянні з іншими діелектриками невелика і їх діелектрична стала коливається у вузьких межах. Пробивна напруга нафтопродуктів залежить від багатьох факторів – вологості, домішок, температури, тиску.
За фізичними і хімічними властивостями нафти розрізняють три види її складу: елементний, фракційний та груповий хімічний.
Елементний склад нафти. Склад і властивості нафт залежать від родовища і можуть коливатися у доволі широких межах.
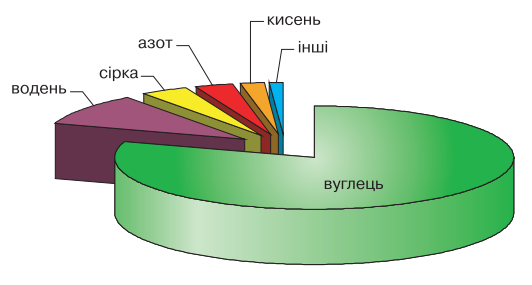 Мал. 8.3. Хімічний склад нафти
Мал. 8.3. Хімічний склад нафти
Численними хімічними аналізами встановлено, що нафта складається головним чином з вуглецю і водню – відповідно 79,5–87,5 і 11,0–14,5% від маси (мал. 8.3). Окрім них, у нафтах присутні ще три елементи – сірка, кисень і азот. Їх загальна кількість звичайно складає 0,5–8%. У дуже незначних концентраціях в нафтах зустрічаються метали – ванадій, нікель, залізо, алюміній, мідь, магній, барій, стронцій, марганець, хром, кобальт, молібден, калій, натрій, цинк, кальцій, срібло, галій та ін., а також бор, миш'як, йод. Загальний склад металів у нафті рідко перевищує 0,02–0,03% від її маси.
Вказані елементи утворюють різноманітні класи хімічних сполук, з яких і складаються нафти.
Вуглеводні являють собою головний клас хімічних сполук в нафтах. Виявлені вони у складі нафт у 1817 р. швейцарським природознавцем Н. Сосюром.
У табл. 8.1 наведено елементний склад деяких горючих копалин.
Поряд з вуглеводнями в нафтах присутні інші хімічні сполуки.
Сірка міститься майже у всіх нафтах. Типи сірчаних сполук в них дуже різноманітні. Окремі нафти містять вільну сірку, яка при тривалому зберіганні випадає в резервуарах у вигляді аморфної маси. В інших випадках сірка знаходиться в нафтах і нафтопродуктах у зв'язаному стані, тобто у вигляді сірководню і сіркоорганічних сполук (меркаптанів, сульфідів і т.ін.).
Основна маса сірчистих сполук нафти має значну молекулярну вагу і високу температуру кипіння. Тому від 70 до 90% всіх сірчистих сполук зосереджується в мазуті та гудроні.
Нафта, яка видобувається на промислах, містить розчинені гази, механічні домішки у вигляді піску і глини (до 0,15%), воду (до 50% і більше), солі (від 0,0001 до 10 г/дм3). Для збільшення нафтовіддачі нафтового пласту, запобігання корозії оснащення, відкладання парафінів і солей використовуються спеціальні способи. У нафту можуть потрапляти небажані компоненти. Тому з метою забезпечення необхідної якості нафти для її подальшого транспортування і переробки на промислах проводиться відповідна підготовка (стабілізація, зневоднення, знесолювання нафти та ін.).
Таблиця 8.1. Елементний склад деяких горючих копалин, %
|
Копалини |
Вуглець |
Водень |
Кисень, сірка та ін. |
|
Нафта |
79,5 – 87,5 |
11,0 – 14,5 |
0,5 – 8,0 |
|
Сланці |
76,6 |
9,2 |
14,2 |
|
Торф сухий |
57,7 |
6,1 |
36,2 |
|
Вугілля: |
|||
|
кам'яне |
81,3 |
5,2 |
13,5 |
|
буре |
74,8 |
5,1 |
20,1 |
Фракційний склад нафти. Нафта і нафтопродукти звичайними методами перегонки неможливо розділити на індивідуальні сполуки. Це робиться шляхом перегонки на окремі частини, будь-яка з яких є менш складною сумішшю. Такі частини називаються фракціями, або дистилятами. Фракція – це група вуглеводнів, яка википає в певному інтервалі температур.
Нафтові фракції на відміну від індивідуальних сполук не мають постійної температури кипіння. Вони википають в певних інтервалах температур, тобто мають температуру початку і закінчення кипіння. Ці обидві температури залежать від хімічного складу фракції.
Фракційний склад нафт і нафтопродуктів показує вміст в них різноманітних фракцій, що википають в певних температурних межах.
Для визначення фракційного складу нафт і їх окремих частин у лабораторній практиці найбільш поширеними стали наступні методи перегонки.
1. Низькотемпературна ректифікація – для зріджених газів і фракцій вуглеводнів, що киплять при температурі нижче 20°С.
2. Середньотемпературна перегонка – для нафтопродуктів, що википають при температурі до 350°С.
3. Вакуумна перегонка – для рідин, що википають при температурі вищій 350°С.
4. Молекулярна дистиляція – для високомолекулярних речовин.
5. Перегонка методом одноразового випарювання.
При розділенні нафти в лабораторних умовах в інтервалі температур від 40 до 180–205°С відбирають бензинові фракції, причому отриману при 160–205°С називають лігроїновою фракцією, а при 40–70 і до 90°С – петролейним ефіром; в інтервалі температур від 200 до 300°С отримують керосинові фракції; при 270–350°С – газойлеву (газойль); при 300–370°С – солярову.
Після відгону з нафти всіх цих фракцій залишається в'язка темна рідина, яка зветься мазутом. Тривалий час, до кінця ХІХ ст., мазут в промисловості не використовувався: він належав до відходів нафтопереробки. Це пояснюється значними труднощами подальшої його переробки, пов'язаними з тим, що температура перегонки мазутних фракцій при атмосферному тиску вища, ніж температура їх термічної деструкції, тобто розриву молекул на частинки під впливом температури. Розділити мазут на фракції вдалося лише при зниженні тиску. Цей процес, який називається вакуумним, дозволив отримати з мазуту солярові фракції і спеціальні масла (легкі, середні та в'язкі), у тому числі масла для двигунів внутрішнього згоряння.
У промислових умовах перегонка нафти здійснюється не послідовним випарюванням (як на лабораторних апаратах), а одноразовим випарюванням з подальшою ректифікацією. При цьому відбирають наступні світлі фракції (дистиляти): бензинову (до 180°С), керосинову (120–315°С), дизельну, або керосино-газойлеву (180–350°С), різноманітні проміжні фракції. Світлі дистиляти за допомогою наступної очистки, змішування, а іноді й вторинної перегонки перетворюються в товарні продукти прямої перегонки нафти.
До світлих товарних нафтопродуктів прямої перегонки відносяться бензини (авіаційний, автомобільний), розчинники й керосини (освітлювальний і для технічних цілей). Темний продукт, що називається мазутом, і залишок, який отримують в результаті прямої перегонки нафти при температурі вищій 300–350°С, переробляються шляхом розгонки під вакуумом з метою отримання масляних дистилятних масел.
Дистилятні масла (авіаційні; автомобільні; автотракторні дизельні; індустріальні – машинні трансформаторні, турбінні, циліндрові; білі масла – парфумерне і вазелінове медичне – та ін.), що утворюються після розгонки мазуту, відбираються вже не за температурою кипіння і густиною, а за величиною їх в'язкості.
Залишок після перегонки мазуту (при температурі вище 500°С) називається гудроном або напівгудроном залежно від в'язкості й використовується для приготування високов'язких мастил, будівельних і дорожніх матеріалів (бітуми нафтові).
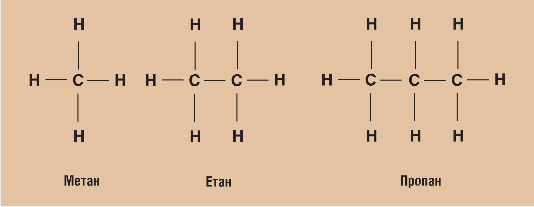 Мал. 8.4. Структурні формули метанових вуглеводнів
Мал. 8.4. Структурні формули метанових вуглеводнів
Перегонці на масла піддаються лише мазути так званих «масляних нафт». У низці випадків мазути таких «масляних нафт» використовуються самостійно (без перегонки на масла) чи в суміші з іншими нафтопродуктами як мастильні мазути, тобто дешеві мастильні матеріали. Значно більше мазуту використовується як паливо, в тому числі для суднових двигунів. Особлива велика кількість мазуту служить сировиною для переробки на легкі моторні палива.
Нафти різних родовищ дуже відрізняються одна від одної за фракційним складом, а звідси – і за потенційним вмістом бензинових, керосинових, дизельних і масляних дистилятів. Очевидно, що фракційний склад нафти визначає шляхи її промислової переробки.
Більшість нафт містять в середньому 15–30% фракцій, які википають при температурі до 200°С, 40–50% фракцій, які переганяються в інтервалі 300–360°С.
Легкі нафти, що не містять масляних фракцій, зустрічаються рідко. Здебільшого вони є супутниками газів у газоконденсатних родовищах і їх називають газоконденсатами.
Груповий хімічний склад нафти. Вуглеводні, які складають основу нафти і горючих газів, представлені багатьма індивідуальними сполуками. Хімічний склад нафти до кінця не відомий, але вже встановлено 425 вуглеводневих сполук, кожна з яких у свою чергу є вихідною для більш складних сполук. У залежності від будови молекул вуглеводні, що входять до складу нафт і природних газів, поділяються на три основні групи: метанові, чи парафінові (алкани), нафтенові (циклани) і ароматичні (арени). Представники цих груп відрізняються один від одного співвідношенням числа атомів вуглецю і водню, яке відображається загальною формулою групи, і характером їх внутрішніх структурних зв'язків.
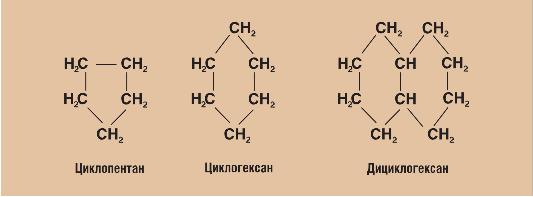 Мал 8.5. Структурні формули нафтенових вуглеводнів
Мал 8.5. Структурні формули нафтенових вуглеводнів
Таким чином, груповим хімічним складом нафти називають вміст у ній вуглеводнів певних хімічних груп, які характеризуються співвідношенням і структурою сполук атомів вуглецю і водню.
Метанові вуглеводні (алкани) – насичені вуглеводні, в яких відсутні подвійні зв'язки. Загальна формула СnН2n+2, де n – число атомів вуглецю. Таке атомарне співвідношення вуглецю і водню у вуглеводнях цієї групи було встановлене англійськими хіміками ще в 1833 р. У зазначеній формулі n змінюється від 1 до 60. Це означає, що в природі існує послідовний ряд метанових вуглеводнів, що поступово ускладнюються.
Кожний наступний член у цьому ряду відрізняється від попереднього на один атом вуглецю і два атоми водню. Подібний ряд називається гомологічним (грецьк.«хомос» – схожий), а його члени – гомологами.
Існування гомологічних рядів для вуглеводневих сполук було виявлено у 1843 р. видатним французьким хіміком Шарлем Фредеріком Жераром. Це відкриття мало велике значення для розуміння закономірностей зміни складу нафт.
Для вуглеводнів метанового ряду характерне утворення відкритих ланцюжків, які збільшуються (мал. 8.4).
У молекулах вуглеводнів метанового ряду валентність всіх атомів вуглецю насичена до межі, тому метанові вуглеводні називаються насиченими, чи граничними. Внаслідок цього вони мають малу хімічну активність. Звідси пішла ще одна їх назва – парафінові (лат. «парум аффініс» – малоспоріднений, тобто інертний, не схильний до реакцій) вуглеводні. Парафінами називається суміш вуглеводнів метанового ряду з молекулярною масою від 240 і вище. Вміст парафінових вуглеводнів у нафтах коливається від частки відсотка до 20% і більше.
У залежності від молекулярної маси і хімічної структури метанові вуглеводні знаходяться в газоподібній, рідкій і твердій фазах. Так, перші чотири члени ряду (метан, етан, пропан, бутан) за нормальних умов (101,32 кПа и 0°С) – гази, вуглеводні від пентану до пентадекану C15H32 за тих же умов – рідини, а від гексадекану C16H34 і вище – тверді речовини.
Нафтенові вуглеводні (циклани) були відкриті у 80-ті роки позаминулого століття російським вченим В.В.Марковніковим. Їх спільна формула СnН2n. Молекули нафтенових вуглеводнів складаються з декількох метиленових груп – СН2, з'єднаних у замкнуте кільце, чи цикл (мал. 8.5).
Тому такі вуглеводні називають ще поліметиленовими, або цикланами (грецьк. «циклос» – коло). Нафтенові вуглеводні, як і метанові, є насиченими. Молекули можуть складатися з одного чи двох, трьох і більше об'єднаних метиленових кілець.
У нафті містяться переважно нафтени, кільця яких складаються з п'яти чи шести груп – СН2. До кілець – циклів – можуть приєднуватися і бокові ланцюжки метанової будови. У цьому випадку атом водню в метиленовій групі =СН2 буде заміщений на будьякий вуглеводневий радикал – метил СН3, етил C2H5 та ін. Таким чином, без розриву нафтенового кільця виходять нові вуглеводні – похідні циклопентану і циклогексану. Ними можуть бути, наприклад, метилциклопентан, чи метилпентаметилен (C6H12), етилциклогексан, чи етилгексаметилен (C8H16) та ін.
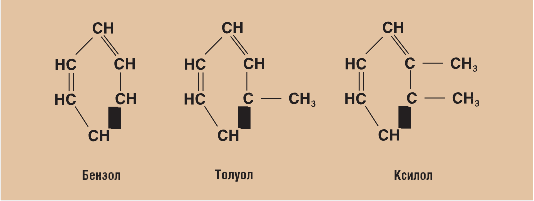 Мал. 8.6. Структурні формули ароматичних вуглеводнів
Мал. 8.6. Структурні формули ароматичних вуглеводнів
Таблиця 8.2. Вміст вуглеводневих фракцій, %
|
Регіони розміщення нафтових родовищ |
Парафінові фракції |
Нафтенові фракції |
Ароматичні фракції |
|
Прикарпаття |
47–49 |
26–35 |
18–25 |
|
Дніпровсько-Донецька западина |
28–66 |
22–53 |
12–33 |
|
Білорусь |
60–71 |
13–27 |
11–21 |
|
Литва |
73–74 |
22–23 |
4–5 |
|
Азербайджан (материк) |
28–56 |
39–68 |
2–17 |
|
Азербайджан (море) |
35–56 |
27–60 |
1–20 |
|
Дагестан |
58–62 |
25–31 |
11–13 |
|
Чечено-Інгушетія |
51–61 |
16–41 |
8–28 |
|
Калінінградська область |
70–74 |
21–26 |
4–5 |
|
Краснодарський край |
20–47 |
42–56 |
11–50 |
|
Ставропольський край |
51–65 |
20–37 |
12–15 |
Нафтенові вуглеводні – важлива складова частина моторного палива і масел. Автомобільним бензинам вони надають високих експлуатаційних властивостей.
Нафтенові вуглеводні легких фракцій нафт широко використовуються як сировина для отримання ароматичних вуглеводнів, бензолу і толуолу, а нафтенові вуглеводні бензинових фракцій у процесі каталітичного риформінгу перетворюються в ароматичні.
Ароматичні вуглеводні – одна з найбільш важливих і обширних груп вуглеводнів. Їх формула СnН2n–m, де n починається з 6, m може бути виражене парними числами від 6 і більше. У структурному відношенні молекула ароматичних вуглеводнів має вигляд замкнутого кільця (циклу), яке об'єднує радикали – СH (мал.8.6).
На відміну від молекули нафтенів в ароматичному кільці атоми вуглецю через один з'єднані не одинарними зв'язками, а подвійними. Тому ароматичні вуглеводні є ненасиченими (неграничними) сполуками, але в той же час внаслідок замкнутої циклічної (кільцевої) будови вони малоактивні. Для них характерні реакції заміщення атомів водню атомами інших елементів – хлору, брому, йоду та ін.
Найпростіша будова серед ароматичних вуглеводнів характерна для бензолу С6Н6 (кільце – «шестикутник»). Інші відомі ароматичні вуглеводні є, по суті, його похідними.
У порівнянні з іншими групами вуглеводнів ароматичні мають найбільшу густину. За в'язкістю вони займають проміжне становище між парафіновими та нафтеновими.
Ароматичні вуглеводні – цінні компоненти бензинів, однак вони знижують якість реактивних та дизельних палив, оскільки погіршують характеристики їх згоряння.
Ненасичені вуглеводні (алкени, алкадієни) зустрічаються в нафтах дуже рідко і в невеликих кількостях.
У табл. 8.2 на прикладі нафт деяких родовищ наведені узагальнені показники вмісту парафінових, нафтенових і ароматичних фракцій.
Раздел 7. Уголь
8.1. История открытия и использования нефти и газа и их происхождение



